5月2日,中國(guó)生物發(fā)布消息,,由國(guó)藥集團(tuán)中國(guó)生物北京生物制品研究所研發(fā)的奧密克戎變異株新冠病毒滅活疫苗序貫免疫臨床研究,,于5月1日在浙江省杭州市完成第一劑接種。這是全球首支進(jìn)入臨床試驗(yàn)的,,針對(duì)奧密克戎變異株的新冠病毒滅活疫苗,。
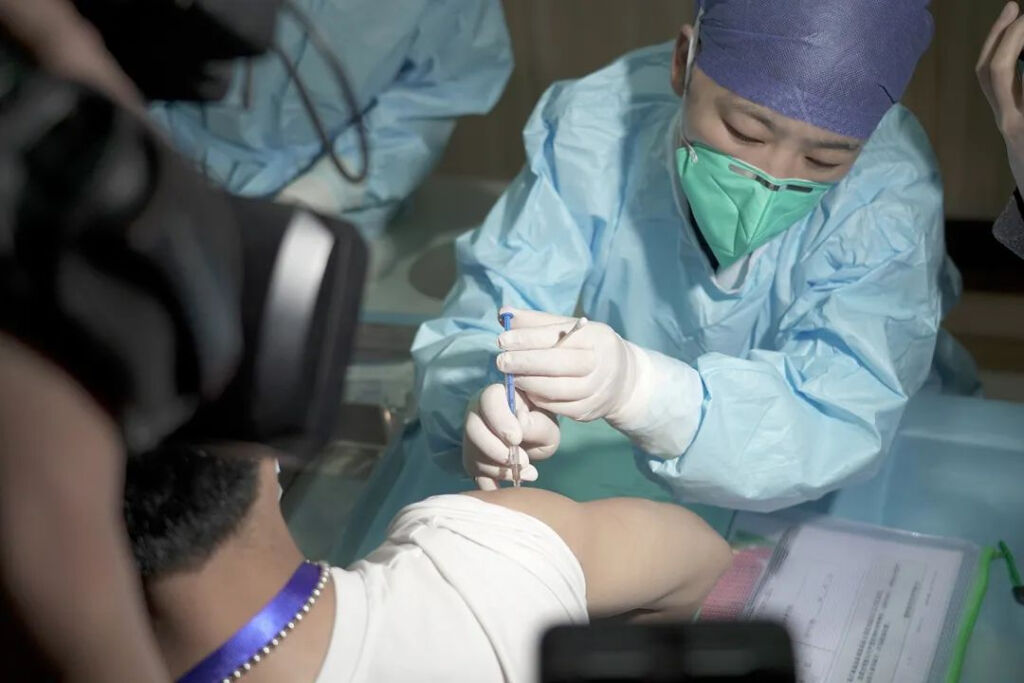
此次奧株新冠疫苗臨床研究將采用隨機(jī)、雙盲,、隊(duì)列研究的形式,,在已完成2或3劑新冠疫苗接種的18歲及以上人群中進(jìn)行序貫免疫臨床研究,評(píng)價(jià)奧密克戎變異株新冠病毒滅活疫苗的安全性和免疫原性,。
國(guó)藥集團(tuán)總工程師,、中國(guó)生物董事長(zhǎng)楊曉明表示,奧密克戎變異株傳染性極強(qiáng),、傳播速度極快,,多為隱匿傳播,中國(guó)生物研發(fā)團(tuán)隊(duì)與病毒拼強(qiáng)度,、拼速度,,第一時(shí)間研發(fā)出奧株新冠疫苗,并完成工藝驗(yàn)證,、多批規(guī)?;a(chǎn)品的制備、質(zhì)量標(biāo)準(zhǔn)研究、動(dòng)物體內(nèi)安全性評(píng)價(jià)和免疫原性研究,,現(xiàn)已進(jìn)入最為關(guān)鍵的臨床試驗(yàn)階段,。
中國(guó)生物首席科學(xué)家、副總裁張?jiān)茲硎?,奧株新冠疫苗臨床試驗(yàn)的啟動(dòng)中國(guó)生物在抗擊新冠領(lǐng)域取得的又一重要進(jìn)展,。此次臨床試驗(yàn)將在已接種2或3針新冠疫苗,及在未接種新冠疫苗的空白人群中開(kāi)展,,從而觀察疫苗的安全性和免疫原性,。
據(jù)悉,中國(guó)生物在前期已上市原型株新冠滅活疫苗和完成貝塔,、德?tīng)査儺愔隃缁钜呙缪邪l(fā)的基礎(chǔ)上,,第一時(shí)間從香港大學(xué)引進(jìn)奧密克戎變異毒株,2021年12月9日迅速啟動(dòng)了奧株疫苗研發(fā),。
4月12日,,中國(guó)生物北京生物制品研究所、武漢生物制品研究所研發(fā)的兩款?yuàn)W株新冠病毒滅活疫苗獲得香港大學(xué)及醫(yī)管局港島西醫(yī)院聯(lián)網(wǎng)研究倫理委員會(huì)的審查同意,,并于4月13日獲得香港藥劑業(yè)及毒藥管理局的臨床試驗(yàn)批件,,正式獲準(zhǔn)在香港開(kāi)展新冠疫苗的序貫免疫臨床研究。
4月26日,,中國(guó)生物北京生物制品研究所奧株新冠病毒滅活疫苗獲得國(guó)家藥監(jiān)局臨床試驗(yàn)批件,。
4月29日,中國(guó)生物北京生物制品研究所,、武漢生物制品研究所兩款?yuàn)W株新冠病毒滅活疫苗及國(guó)藥中生生物技術(shù)研究院/新型疫苗國(guó)家工程研究中心研發(fā)的重組新冠疫苗,,共計(jì)三款?yuàn)W株新冠疫苗獲阿聯(lián)酋阿布扎比衛(wèi)生部臨床試驗(yàn)批件,。這是中國(guó)生物奧株新冠疫苗全球多中心臨床試驗(yàn)的重要進(jìn)展,。下一步,中國(guó)生物將積極深入高效推進(jìn)各條技術(shù)路線奧株新冠疫苗的臨床試驗(yàn)工作,。
(責(zé)編:劉予欣)












